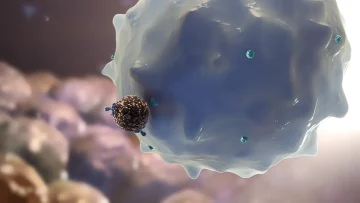
Un macrófago a punto de fagocitar a un intruso. Foto: Shutterstock.
Por Estanislao Nistal Villán y Sara Cuadrado Castaño PhD / The Conversation
Cada día, los seres humanos nos defendemos frente a microorganismos nocivos de forma “silenciosa”. Estas batallas que ganamos –en muchas ocasiones de manera inadvertida– son el resultado de una larga historia de coexistencia y evolución con numerosos patógenos. La exposición a ellos ha educado a nuestro sistema inmunitario para reconocer y contrarrestar la infección y prevenir la enfermedad.
Enfrentarnos a agentes infecciosos es uno de los estímulos que refuerza nuestra capacidad de defensa, a veces más allá de lo que imaginamos. Y lo que ocurre cuando el organismo lucha contra la gripe puede servir de ejemplo.
Sesión de entrenamiento inmunitario
La gripe es una enfermedad producida por cuatro tipos de virus, pertenecientes a la familia Orthomyxoviridae, que se clasifican según las características de su genoma. A los humanos les afectan principalmente los virus de gripe de tipo A y tipo B.
A pesar de su riesgo letal, enfrentarnos a estos virus y vencer a la enfermedad puede tener un lado positivo.
Curarnos de la gripe puede compararse a realizar un entrenamiento que nos sirve para superar una prueba concreta y saber cómo superarla mejor en el futuro. Pero además va a adiestrar a nuestro sistema inmunitario para enfrentarnos a amenazas similares, como otros virus de la gripe, y bastante diferentes, como otros virus respiratorios o incluso el cáncer.
Entrenar nuestras defensas de forma no específica es un concepto conocido desde hace tiempo, pero qué determina su activación y sus efectos son tema de estudio actualmente.
Un marcapáginas en el ADN
El sistema inmunitario se puede clasificar en dos grandes grupos, el adaptativo y el innato. Mediante las vacunas entrenamos preferentemente el primero. En cambio, para ejercitar el sistema innato es necesario activar las células que lo componen o sus precursoras: los monocitos, las células NK, los macrófagos, las células linfoides innatas, las células dendríticas y los neutrófilos. La instrucción de estas células se traduce en una memoria inmune innata o inmunidad entrenada.
Sustancias procedentes de microorganismos o compuestos producidos por nuestras células durante una infección pueden estimular la inmunidad innata para que reaccione frente a lo que es percibido como una agresión mediante la expresión de ciertos genes. Este estímulo deja una huella en el ADN, como si se tratase de un marcapáginas en un libro que hemos leído previamente.
Los “marcapáginas” se producen en forma de metilaciones en el ADN de las células de la inmunidad innata y modificaciones de histonas, las proteínas que empaquetan este ADN. Actúan como señaladores para localizar más eficazmente determinados genes en caso de que nuestras células de inmunidad innata vuelvan a ser estimuladas.
Este marcaje puede facilitar una respuesta más rápida y eficaz frente a infecciones futuras, pero también puede desencadenar una sobrerrespuesta inflamatoria con efectos perjudiciales.
Los efectos antitumorales de pasar la gripe (en ratones)
Un artículo publicado recientemente en la revista Nature describía un proceso de inmunidad entrenada inducido por una infección. Los investigadores inocularon a ratones un virus de gripe que no llegaba a ser letal. Un mes más tarde, y tras haberse recuperado de la infección, los animales fueron tratados para que generaran tumores pulmonares.
Y sorprendentemente, los ratones recuperados de la gripe desarrollaban los tumores más lentamente que los no infectados con antelación.
La mejor protección antitumoral se debe a la estimulación de la inmunidad entrenada de un tipo de células denominadas macrófagos alveolares. Estas células son las responsables de limpiar y eliminar partículas o microorganismos que entran en nuestros pulmones cuando respiramos, y controlan la inflamación que se genera al reconocer un agente extraño.
Durante una infección aguda, muchos macrófagos alveolares mueren, pero los recuperamos posteriormente. Esa recuperación viene marcada por la presencia de los “marcapáginas” en algunos genes inflamatorios.
El entrenamiento de estos macrófagos depende de otras compañeras, las células NK. Estas actúan como instructoras durante la infección por el virus de la gripe produciendo una citoquina (proteína que regula la respuesta inmunitaria) denominada interferón gamma.
Esta citoquina es como un bálsamo de Fierabrás para los macrófagos alveolares: estimula su capacidad de engullir y digerir para destruir las células tumorales, algo que también podría mejorar la activación de la respuesta inmune adaptativa.
Este descubrimiento no supone una solución a corto plazo para tratar el cáncer de pulmón, o de los tumores en general. No obstante, pone el foco en dos ideas que pueden revolucionar el tratamiento de algunos tumores: los virus con actividad inmunoestimuladora oncolítica –capaces de activar el sistema inmune para destruir selectivamente células tumorales– y la estimulación de la inmunidad innata antitumoral.
En los años 50 y 60 del siglo pasado, la doctora Alice Moore fue una pionera en estudiar los virus oncolíticos en modelos animales. Nos encontramos en los albores de su uso para que el sistema inmunitario humano ataque y destruya específicamente a células tumorales. En este reto se encuentra la siguiente frontera de la inmunoterapia antitumoral.
Estanislao Nistal Villán, Virólogo y profesor de Microbiología de la Facultad de Farmacia, Universidad CEU San Pablo and Sara Cuadrado Castaño PhD, Research Assistant Professor, Icahn School of Medicine at Mount Sinai
Este artículo fue publicado originalmente en The Conversation. Lea el original.